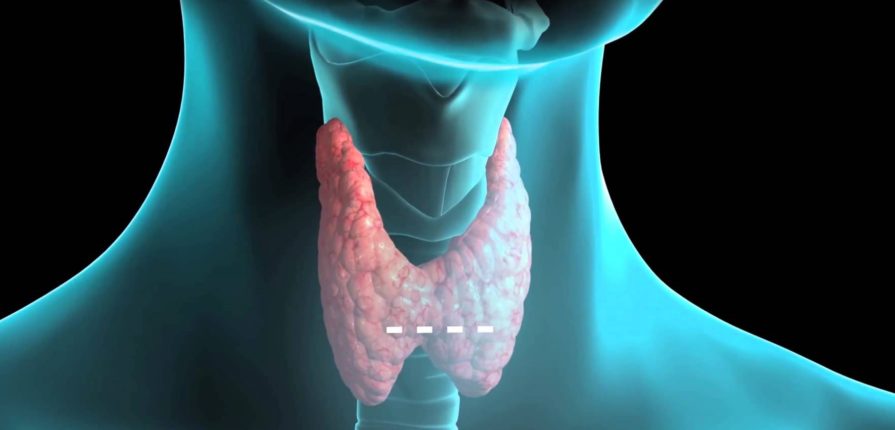
La tiroide con la sua produzione ormonale è tra tutte le ghiandole endocrine il “master regolatore” del metabolismo. Perché possa lavorare al meglio ha bisogno
- dell’azione del TSH ipofisario
- dell’aminoacido tirosina
- di un adeguato apporto in iodio
- dell’enzima tireo-perossidasi (TPO, quella contro la quale si sviluppano gli auto-anticorpi)
- e del selenio (che come vedremo è necessario per la conversione del T4 a T3).
La tiroide è formata da una serie di concamerazioni che chiamiamo follicoli tiroidei. Le cellule epiteliali di ciascun follicolo sintetizzano la tireoglobulina, gliocoproteina dimerica e principale costituente della sostanza colloidale che si trova nel lume follicolare.
La TPO catalizza la reazione che rende possibile incorporare lo iodio inorganico nello scheletro della tireoglobulina proprio a livello dei residui di tirosina. A seconda di quanti atomi di iodio vengono inseriti nella molecola avremo la produzione di T1, T2, T3, T4 (contenenti rispettivamente 1, 2, 3 e 4 atomi di iodio).
La tiroide sintetizza in massima parte T4 mentre il grosso del T3 viene prodotto al di fuori della ghiandola per trasformazione del T4 ad opera di un enzima chiamato 5-deiodinasi. Questo enzima non fa altro che togliere un atomo di iodio dalla molecola del T4 che diventa così T3.
Ed è proprio perché la 5-deidoninasi contiene selenio che la presenza di questo minerale in quantità adeguate diviene indispensabile ai fini della produzione di T3. Quando per un’anomalia del Sistema Immunitario si producono autoanticorpi (in particolare anti-tireoperossidasi e anti-tireoglobulina) la sintesi di ormoni tiroidei non sarà più adeguata. Si parla allora di tiroidite di Hashimoto.
Alcuni Autori si sono chiesti se il microbiota intestinale possa avere un ruolo di corresponsabilità nel determinismo di questa malattia (1, 2).
Una sana flora batterica intestinale, con i batteri buoni che prevalgono sui batteri cattivi, è fondamentale al fine di realizzare la piena omeostasi digestiva ed immunologica. Al contrario in condizioni di disbiosi, con i batteri cattivi che prendono il sopravvento, la mucosa intestinale subisce danni strutturali e diviene permeabile al passaggio di antigeni batterici ed alimentari. Si parla in tal caso di leaky gut syndrome, per l’appunto sindrome dell’intestino permeabile. In questa condizione la barriera mucosale è distrutta e gli antigeni approdano a livello della sottomucosa entrando così in relazione con il Sistema Immunitario. A livello istologico si evidenzia la presenza di un infiltrato linfocitario intraepiteliale. A livello sistemico non è infrequente la comparsa di patologie auto-immuni quali il diabete mellito di tipo 1, l’artrite reumatoide e la tiroidite di Haschimoto.
Ma l’intestino con il suo immenso carico microbico potrebbe avere altre responsabilità nel determinare stati di ipotiroidismo.
Da diversi anni si conosce un altro derivato endogeno degli ormoni tiroidei, la 3 iodotironamina (in sigla T1AM). La sua struttura molecolare differisce da quella del T3 e del T4 per l’assenza di un gruppo carbossilico (è dalla deiodinazione e dalla decarbossilazione enzimatica di T4 che si ottiene T1AM). Se somministrata a dosi farmacologiche la T1AM ha effetti acuti e drammatici sulla frequenza cardiaca, sulla temperatura corporea e sulle funzioni neuro-cognitive inducendo uno stato di generale torpore (tutto questo somiglia tanto al quadro clinico di un ipotiroidismo). Recentemente alcuni Autori hanno dimostrato che la biosintesi del T1AM avviene per la gran parte a livello intestinale (3).
Quanto ho scritto fin qui fa parte delle nostre conoscenze consolidate. Quella che sto per scrivere è invece soltanto un’ipotesi. Pensate all’insieme dei batteri intestinali immersi in un sistema tanto complesso da meritarsi il nome di “secondo cervello”. È un po’ come stare nella sala di comando di un’astronave. Sai che pigiando un bottone hai il potere di regolare l’intero sistema. Di certo i nostri batteri, abitando il nostro intestino da milioni di anni, sanno bene quali bottoni pigiare. I batteri cattivi potrebbero ad esempio favorire la biosintesi del T1AM ottenendo così un rallentamento della peristalsi intestinale e di tutte le funzioni in generale. Questo gli consentirebbe di avere per sé la gran parte dei nutrienti ingeriti dal loro ospite.
Si tratta ovviamente solo di un’ipotesi ma non è forse grazie alle ipotesi che le nostre conoscenze evolvono?
Non siamo ancora in grado di dominare l’immensa complessità del sistema uomo-microbiota ma ci rendiamo finalmente conto che non si possono curare le malattie concentrando l’attenzione solo sull’organo colpito.
Bibliografia
- Virili C, Centanni M. Does microbiota composition affect thyroid homeostasis? Endocrine 2015; 49(3):583-7.
- Mori K et al. Does the gut microbiota trigger Hashimoto’s Thyroiditis? Discov Med 2012; 14(78):321-6.
- Hoefig CS et al. Biosynthesis of 3-Iodothyronamine froma T4 in murine intestinal tissue. Endocrinology 2015; 156(11):4356-64.

Lascia un commento